식약처, 회수·폐기 처분 돌입…소비자 보호 차원서 ‘사용 중지’ 조치도
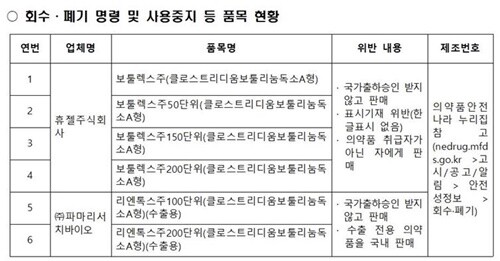 <자료=식품의약품안전처>
<자료=식품의약품안전처>
휴젤‧파마리서치바이오의 보툴리눔 제제가 품목허가 취소 위기에 놓였다.
10일 식품의약품안전처에 따르면 휴젤‧파마리서치바이오 등 2개 업체가 국가출하승인을 받지 않고 보툴리눔 제제 6개 품목을 국내에 판매한 사실을 적발해 이들 제품에 대한 품목허가 취소 절차에 착수했다.
이번에 적발된 국가출하승인 위반 품목은 ▲파마리서치바이오 리엔톡스주100단위 ▲리엔톡스주200단위 ▲휴젤의 보툴렉스주 ▲보툴렉스주50단위 ▲보툴렉스주150단위 ▲보툴렉스주200단위다.
특히 파마리서치바이오 2개 제품은 수출 전용 의약품인데도 국내 판매용 허가 없이 판매한 것으로 적발돼 제조업무정지 6개월 처분도 받게 된다.
‘보톡스’로 통칭되는 보툴리눔 제제는 미간 주름 개선 등 미용성형 시술에 주로 쓰이는 바이오의약품이다.
보툴리눔 제제나 백신 등 보건위생상 특별한 주의가 필요한 생물학적 제제는 품목허가를 받았더라도 이와 별도로 시판되기 전 식약처로부터 품질 등을 확인받는 국가출하승인을 받아야 한다.
식약처는 행정처분 절차 착수와 함께 문제가 된 품목이 국내에 유통되지 않도록 회수·폐기 명령을 내렸다. 동시에 행정절차 상 시간이 걸리는 것을 고려해 소비자 보호 차원에서 사용 중지 조치를 내린 상태다.
또 의·약사 등에게 이 품목을 다른 제품으로 대체하고 제품 회수가 적절히 이뤄질 수 있도록 협조를 요청하는 안전성 속보를 배포했다. 보건복지부와 건강보험심사평가원에는 병·의원이 이 해당 품목을 사용하지 않도록 안내해 줄 것을 요청했다.
토요경제 / 김동현 기자 coji11@sateconomy.co.kr
[저작권자ⓒ 토요경제. 무단전재-재배포 금지]





































