[토요경제=이경화 기자] 앞으로 희귀의약품의 경우 임상시험계획 승인만으로도 지정이 가능해진다. 희귀·난치 질환치료제의 신속한 개발을 지원하기 위해서다.
18일 식품의약품안전처는 이 같은 내용의 ‘희귀의약품 지정에 관한 규정’ 개정안을 행정 예고했다.
희귀의약품은 적용대상이 드물고 적절한 대체의약품이 없어 긴급한 도입이 필요한 의약품을 말한다.
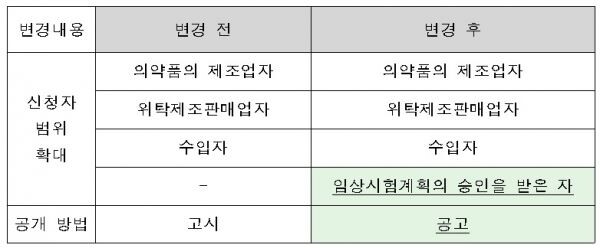
주요 내용은 희귀의약품 지정 신청자 범위 확대, 희귀의약품 지정 절차 변경을 통한 공개방법 개선 등이다.
이에 따라 기존에는 의약품 제조업·위탁제조판매업·수입자만 희귀의약품으로 지정받아 제품을 개발할 수 있었던 반면, 앞으로는 임상시험 계획을 승인 받은 경우에도 신청할 수 있도록 했다.
또 희귀의약품은 그 동안 행정예고 등을 거쳐 지정했지만, 식약처 홈페이지를 통해 공고해 지정 기간을 단축할 수 있게 됐다.
[저작권자ⓒ 토요경제. 무단전재-재배포 금지]






































